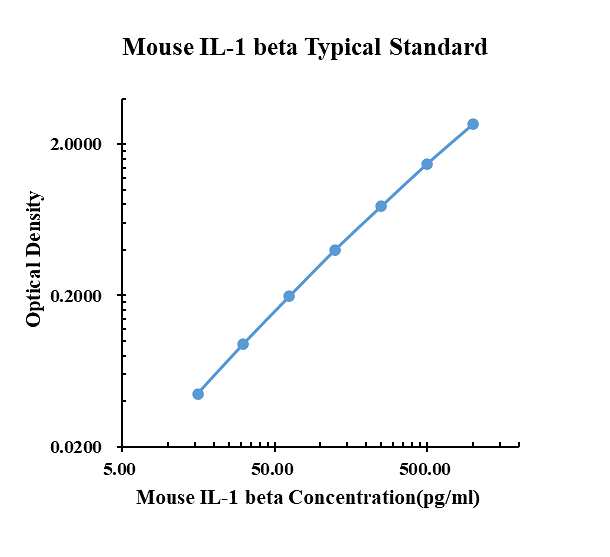
Kit ELISA IL-1β de ratón
IL-1 alfa e IL-1 beta son polipéptidos estructuralmente relacionados que muestran aproximadamente un 25 % de homología a nivel de aminoácidos (aa). Ambos se sintetizan como precursores de 31 kDa que posteriormente se escinden en proteínas maduras de aproximadamente 17,5 kDa. La escisión del precursor IL-1 beta por Caspasa-1/ICE es un paso clave en la respuesta inflamatoria. Ni la IL-1 alfa ni la IL-1 beta contienen un péptido señal hidrofóbico típico, pero la evidencia sugiere que estos factores pueden secretarse por vías no clásicas. Una porción de IL-1 alfa sin procesar puede presentarse en la membrana celular y puede conservar actividad biológica. La forma precursora de IL-1 beta, a diferencia del precursor de IL-1 alfa, muestra poca o ninguna actividad biológica en comparación con la forma procesada. Tanto las formas maduras como las no procesadas de IL-1 beta se exportan desde la célula.
IL-1 alfa e IL-1 beta ejercen sus efectos a través de receptores de la superfamilia de inmunoglobulinas que además se unen a IL-1ra. El receptor transmembrana tipo I de 80 kDa (IL-1 RI) se expresa en células T, fibroblastos, queratinocitos, células endoteliales, células del revestimiento sinovial, condrocitos y hepatocitos. El receptor transmembrana tipo II de 68 kDa (IL-1 RII) se expresa en células B, neutrófilos y células de la médula ósea. Los dos tipos de receptores de IL-1 muestran aproximadamente 28% de homología en sus dominios extracelulares, pero difieren significativamente en que el receptor de tipo II tiene un dominio citoplasmático de sólo 29 aa, mientras que el receptor de tipo I tiene un dominio citoplasmático de 213 aa. IL-1 RII no parece emitir señales en respuesta a IL-1 y puede funcionar como un receptor señuelo que atenúa la función de IL-1. La proteína accesoria del receptor IL-1 (IL-1 RAcP) se asocia con IL-1 RI y es necesaria para la transducción de señales de IL-1 RI. IL-1ra es una molécula secretada que funciona como un inhibidor competitivo de IL-1. Se han detectado formas solubles de IL-1 RI e IL-1 RII en plasma humano, líquidos sinoviales y medios condicionados de varias líneas celulares humanas. Además, los virus vaccinia y de la viruela vacuna codifican proteínas de unión a IL-1 que se asemejan a la IL-1 RII soluble.
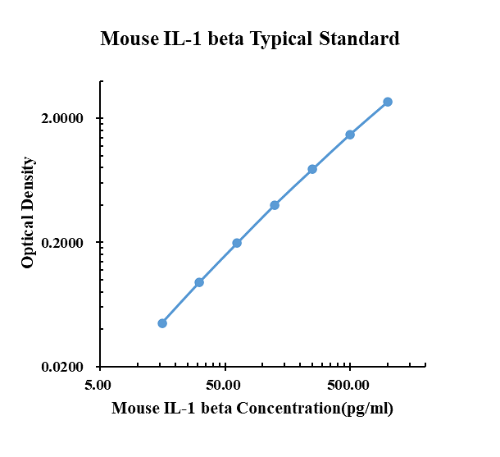
|
pg/ml |
D.O. |
Promedio |
Corregido |
|
|
0.00 |
0.0651 |
0.0701 |
0.0676 |
|
|
15.63 |
0.1104 |
0.1143 |
0.1124 |
0.0448 |
|
31.25 |
0.1660 |
0.1609 |
0.1635 |
0.0959 |
|
62.50 |
0.2623 |
0.2676 |
0.2650 |
0.1974 |
|
125.00 |
0.4740 |
0.4650 |
0.4695 |
0.4019 |
|
250.00 |
0.8593 |
0.8316 |
0.8455 |
0.7779 |
|
500.00 |
1.5070 |
1.6060 |
1.5565 |
1.4889 |
|
1000.00 |
2.7780 |
2.8080 |
2.7930 |
2.7254 |
|
Precisión intra-ensayo |
Precisión inter-ensayo |
|||||
|
Número de muestra |
S1 |
S2 |
S3 |
S1 |
S2 |
S3 |
|
22 |
22 |
22 |
6 |
6 |
6 |
|
|
Promedio (pg/ml) |
18.9 |
93.0 |
290.2 |
17.4 |
97.5 |
280.7 |
|
Desviación estándar |
1.0 |
4.5 |
16.9 |
2.3 |
8.5 |
14.6 |
|
Coeficiente de variación (%) |
5.3 |
4.9 |
5.8 |
6.1 |
6.1 |
5.7 |
Precisión entre ensayos (Precisión entre ensayos) Se analizaron tres muestras de concentración conocida seis veces en una placa para evaluar la precisión intraensayo.
La recuperación osciló entre el 81% y el 111% con una recuperación media general del 98%.
| Matriz de muestra | Muestra evaluada | Rango (pg/ml) | Detectables (%) | Media de detectables (pg/ml) |
|---|---|---|---|---|
| suero | 30 | nd-3.66 | 13 | 1.08 |
Suero/plasma: se evaluaron treinta muestras de ratones aparentemente sanos para detectar la presencia de IL-1β en este ensayo. No se disponía de antecedentes médicos de los donantes. Dakota del Norte. = no-detectable. Las muestras medidas por debajo de la sensibilidad se consideran no detectables.
 Nuevos productos
Nuevos productos