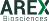Kit ELISA CCL5/RANTES humano
CAT.NO. : AEH0027
US$ Por favor elige
US$ Por favor elige
Tamaño:
Sendero, tamaño a granel o solicitudes personalizadas Por favor contáctenos
Antecedentes
RANTES (regulado tras la activación, expresado y presumiblemente secretado por células T normales), también conocido como CCL5, es un miembro de la subfamilia de quimiocinas "CC". Desempeña un papel principal en la respuesta inmune inflamatoria a través de su capacidad para quimioatraer leucocitos y modular su función. El ADNc de RANTES se descubrió inicialmente mediante hibridación sustractiva como una secuencia específica de células T. El ADNc de RANTES humano codifica un polipéptido precursor de residuos de 91 aminoácidos (aa) altamente básico con un péptido señal hidrofóbico de 23 aa que se escinde para generar la proteína madura de 68 aa. La RANTES humana exhibe aproximadamente un 85% de homología con la RANTES de ratón en el nivel de aa deducido.
RANTES es un potente quimioatrayente para varios tipos de células diferentes, incluidas las células T de memoria CD4+/CD45RO+ no estimuladas y las células T CD4+ y CD8+ estimuladas con fenotipos vírgenes y de memoria, células NK, basófilos, eosinófilos, células dendríticas, mastocitos, monocitos y microglía. Además de sus efectos sobre la migración, RANTES puede activar varios tipos de células, incluidas células T, monocitos, neutrófilos, células NK, células dendríticas y astrocitos. La activación de las células T generalmente requiere concentraciones de RANTES relativamente altas (~ 1 μM) y depende de la agregación de la molécula y la asociación con los glicosaminoglicanos (GAG) de la superficie celular. Aún no está claro si esto [faltan algunas palabras, probablemente 'la actividad ocurre in vivo'], aunque en ratones, los mutantes RANTES inyectados por vía intraperitoneal que son incapaces de agregar y/o unirse a GAG, no son capaces de atraer leucocitos en comparación con los controles de tipo salvaje. Otros estudios in vivo muestran que los ratones knockout para RANTES exhiben un reclutamiento deficiente de leucocitos en sitios de inflamación aguda. - Se sabe que RANTES interactúa con cuatro receptores acoplados a proteína G transmembrana identificados: CCR1, CCR3, CCR4 y CCR5 (22-25). La estimulación RANTES puede iniciar una variedad de cascadas de señalización que dependen del contexto celular. Por ejemplo, en las células T, RANTES puede estimular elevaciones de Ca2+ intracelular y la activación de las vías de señalización de la quinasa de adhesión focal (FAK), la proteína quinasa A, la quinasa PI3, la Rho GTPasa y la JAK/STAT. La proteína US28 del citomegalovirus muestra una homología significativa con los receptores de quimiocinas CC y es capaz de unirse a RANTES. La membrana que abarca US28 puede, dependiendo del contexto, señalar de manera constitutiva, unirse a RANTES e iniciar cascadas de señalización mediadas por proteína G, o secuestrar RANTES y alterar potencialmente las respuestas inflamatorias.
El receptor RANTES CCR5 es también el correceptor principal de las variantes R5 (M-trópicas) del VIH-1. Se ha demostrado que RANTES, así como los otros ligandos de CCR5, la proteína inflamatoria de macrófagos (MIP)-1 alfa y MIP-1 beta, pueden inhibir competitivamente la interacción CCR5/VIH-1 y suprimir la infección viral in vitro. Estos efectos aparentemente no requieren una señalización completamente intacta del receptor CCR5. En consecuencia, las formas modificadas de RANTES y compuestos no peptídicos que bloquean la interacción del VIH-1 con CCR5 son prometedores para terapias futuras. Por el contrario, varios informes muestran que RANTES puede mejorar la replicación in vitro de variantes X4 (T-trópicas) del VIH-1 que utilizan CXCR4 como correceptor en lugar de CCR5. Esta actividad generalmente requiere concentraciones de RANTES relativamente altas (~μM) y depende de la interacción con los GAG de la superficie celular, la oligomerización y la activación de las cascadas de señalización de tirosina quinasa y MAP quinasa.
RANTES es un potente quimioatrayente para varios tipos de células diferentes, incluidas las células T de memoria CD4+/CD45RO+ no estimuladas y las células T CD4+ y CD8+ estimuladas con fenotipos vírgenes y de memoria, células NK, basófilos, eosinófilos, células dendríticas, mastocitos, monocitos y microglía. Además de sus efectos sobre la migración, RANTES puede activar varios tipos de células, incluidas células T, monocitos, neutrófilos, células NK, células dendríticas y astrocitos. La activación de las células T generalmente requiere concentraciones de RANTES relativamente altas (~ 1 μM) y depende de la agregación de la molécula y la asociación con los glicosaminoglicanos (GAG) de la superficie celular. Aún no está claro si esto [faltan algunas palabras, probablemente 'la actividad ocurre in vivo'], aunque en ratones, los mutantes RANTES inyectados por vía intraperitoneal que son incapaces de agregar y/o unirse a GAG, no son capaces de atraer leucocitos en comparación con los controles de tipo salvaje. Otros estudios in vivo muestran que los ratones knockout para RANTES exhiben un reclutamiento deficiente de leucocitos en sitios de inflamación aguda. - Se sabe que RANTES interactúa con cuatro receptores acoplados a proteína G transmembrana identificados: CCR1, CCR3, CCR4 y CCR5 (22-25). La estimulación RANTES puede iniciar una variedad de cascadas de señalización que dependen del contexto celular. Por ejemplo, en las células T, RANTES puede estimular elevaciones de Ca2+ intracelular y la activación de las vías de señalización de la quinasa de adhesión focal (FAK), la proteína quinasa A, la quinasa PI3, la Rho GTPasa y la JAK/STAT. La proteína US28 del citomegalovirus muestra una homología significativa con los receptores de quimiocinas CC y es capaz de unirse a RANTES. La membrana que abarca US28 puede, dependiendo del contexto, señalar de manera constitutiva, unirse a RANTES e iniciar cascadas de señalización mediadas por proteína G, o secuestrar RANTES y alterar potencialmente las respuestas inflamatorias.
El receptor RANTES CCR5 es también el correceptor principal de las variantes R5 (M-trópicas) del VIH-1. Se ha demostrado que RANTES, así como los otros ligandos de CCR5, la proteína inflamatoria de macrófagos (MIP)-1 alfa y MIP-1 beta, pueden inhibir competitivamente la interacción CCR5/VIH-1 y suprimir la infección viral in vitro. Estos efectos aparentemente no requieren una señalización completamente intacta del receptor CCR5. En consecuencia, las formas modificadas de RANTES y compuestos no peptídicos que bloquean la interacción del VIH-1 con CCR5 son prometedores para terapias futuras. Por el contrario, varios informes muestran que RANTES puede mejorar la replicación in vitro de variantes X4 (T-trópicas) del VIH-1 que utilizan CXCR4 como correceptor en lugar de CCR5. Esta actividad generalmente requiere concentraciones de RANTES relativamente altas (~μM) y depende de la interacción con los GAG de la superficie celular, la oligomerización y la activación de las cascadas de señalización de tirosina quinasa y MAP quinasa.
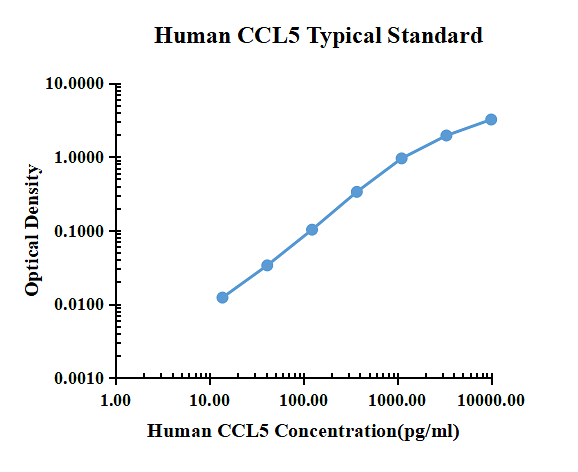
Datos típicos
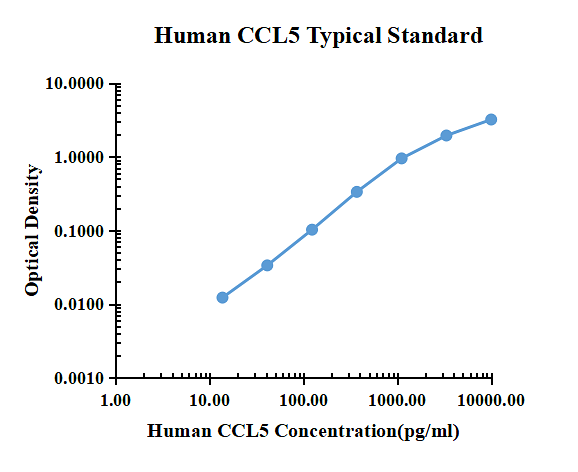
| pg/ml | D.O. | Promedio | Corregido | |
| 0.00 | 0.0151 | 0.0162 | 0.0157 | |
| 13.72 | 0.0271 | 0.0288 | 0.0280 | 0.0123 |
| 41.15 | 0.0489 | 0.0496 | 0.0493 | 0.0336 |
| 123.46 | 0.1175 | 0.1189 | 0.1182 | 0.1025 |
| 370.37 | 0.3486 | 0.3520 | 0.3503 | 0.3346 |
| 1111.11 | 1.0108 | 0.9250 | 0.9679 | 0.9522 |
| 3333.33 | 1.8759 | 2.0533 | 1.9646 | 1.9489 |
| 10000.00 | 3.2985 | 3.1585 | 3.2285 | 3.2128 |
Precisión
| Precisión intra-ensayo | Precisión inter-ensayo | |||||
| Número de muestra | S1 | S2 | S3 | S1 | S2 | S3 |
| 22 | 22 | 22 | 6 | 6 | 6 | |
| Promedio (pg/ml) | 426.6 | 1631.6 | 3396 | 702.2 | 3412 | 8842.1 |
| Desviación estándar | 37.6 | 128.2 | 288.6 | 44.6 | 194.4 | 506.5 |
| Coeficiente de variación (%) | 8.8 | 7.9 | 8.5 | 6.4 | 5.7 | 5.7 |
Precisión intraensayo (Precisión dentro de un ensayo) Se analizaron tres muestras de concentración conocida veinte veces en una placa para evaluar la precisión intraensayo.
Precisión entre ensayos (Precisión entre ensayos) Se analizaron tres muestras de concentración conocida seis veces en una placa para evaluar la precisión intraensayo.
Recuperación de picos
La recuperación del pico se evaluó añadiendo 3 niveles de CCL5 humano a una muestra de suero humano sano. El suero no enriquecido se utilizó como blanco en este experimento.
La recuperación osciló entre el 90% y el 106% con una recuperación media general del 97%.
La recuperación osciló entre el 90% y el 106% con una recuperación media general del 97%.
Valores de muestra
| Matriz de muestra | Muestra evaluada | Rango (pg/ml) | Detectables (%) | Media de detectables (pg/ml) |
| suero | 30 | 943,0-38560,8 | 100 | 21207.7 |
Suero/plasma: se evaluaron treinta muestras de voluntarios aparentemente sanos para detectar la presencia de CCL5 en este ensayo. No se disponía de antecedentes médicos de los donantes.
 Nuevos productos
Nuevos productos




 Folleto de protocolo
Folleto de protocolo