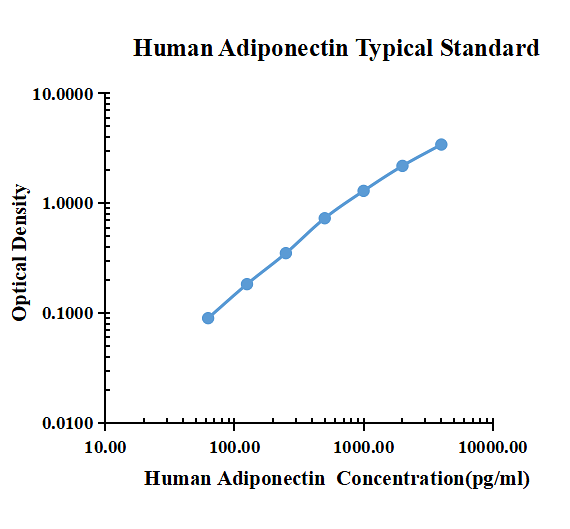
Par de anticuerpos ARExSet® de adiponectina humana para ELISA
La adiponectina, alternativamente denominada proteína relacionada con el complemento de adipocitos de 30 kDa (Acrp30), adipoQ, transcrito 1 del gen adiposo más abundante (apM1) y proteína de unión a gelatina de 28 kDa (GBP28), es una proteína secretada específica de los adipocitos con funciones potenciales en la homeostasis de la glucosa y los lípidos. Los niveles circulantes de adiponectina son altos y representan aproximadamente el 0,01% de la proteína plasmática total. La adiponectina contiene una estructura modular que incluye un dominio similar al colágeno N-terminal seguido de un dominio globular C-terminal con una secuencia significativa y una semejanza estructural con el factor del complemento C1q. Aunque comparten poca identidad de secuencia, una estructura tridimensional similar y ciertos residuos de aminoácidos conservados sugieren un vínculo evolutivo entre el dominio similar a C1q de la adiponectina y los miembros de la superfamilia del TNF. La adiponectina se ensambla en diferentes complejos que incluyen trímeros (bajo peso molecular), hexámeros (peso molecular medio) y estructuras oligoméricas de orden superior (alto peso molecular) que pueden afectar la actividad biológica. La adiponectina se induce durante la diferenciación de los adipocitos y su secreción es estimulada por la insulina. Se han clonado dos receptores de adiponectina, denominados AdipoR1 y AdipoR2. Aunque funcionalmente distintos de los receptores acoplados a proteína G, los genes codifican proteínas predichas que contienen siete dominios transmembrana. AdipoR1 se expresa altamente en el músculo esquelético, mientras que AdipoR2 se encuentra principalmente en los tejidos hepáticos.
La inyección de adiponectina en ratones diabéticos no obesos conduce a una disminución de los niveles de glucosa independiente de la insulina. Esto probablemente se debe a los efectos sensibilizantes a la insulina que implican la regulación de la adiponectina del metabolismo de los triglicéridos. Se ha identificado en la sangre una forma truncada de adiponectina (gAdiponectina) que contiene sólo el dominio globular C-terminal, y se ha demostrado que la gAdiponectina recombinante regula la reducción de peso así como la oxidación de ácidos grasos libres en el músculo y el hígado del ratón. La proteína adiponectina recombinante de longitud completa es aparentemente menos potente para mediar estos efectos. El mecanismo subyacente al papel de la adiponectina en la oxidación de lípidos puede implicar la regulación de la expresión o actividad de proteínas asociadas con el metabolismo de los triglicéridos, incluidas CD36, acil CoA oxidasa, AMPK y PPAR gamma.
Aunque la regulación del metabolismo de la glucosa y los lípidos por adiponectina en humanos es menos clara, también pueden existir mecanismos similares (15. Se ha establecido bien una correlación negativa entre la obesidad y la adiponectina circulante, y los niveles de adiponectina aumentan concomitantemente con la pérdida de peso. Los niveles reducidos de adiponectina se asocian con resistencia a la insulina e hiperinsulinemia, y se informa que los pacientes con diabetes tipo 2 presentan una disminución de la adiponectina circulante. Tiazolidinedionas, una clase de medicamentos antidiabéticos sensibilizantes a la insulina elevan la adiponectina en pacientes resistentes a la insulina. Además, los niveles altos de adiponectina se asocian con un riesgo reducido de diabetes tipo 2. Utilizando espectroscopía de resonancia magnética se ha demostrado que el contenido de lípidos intracelulares en el músculo humano se correlaciona negativamente con los niveles de adiponectina, potencialmente debido a la oxidación de ácidos grasos inducida por la adiponectina.
La adiponectina también puede desempeñar funciones antiaterogénicas y antiinflamatorias. Los niveles plasmáticos de adiponectina disminuyen en pacientes con enfermedad de las arterias coronarias. Además, el engrosamiento neointimal de las arterias dañadas se exacerba en ratones deficientes en adiponectina y es inhibido por la adiponectina exógena. La adiponectina inhibe la expresión de las moléculas de adhesión en las células endoteliales in vitro, suprimiendo la unión de los monocitos. Además, la adiponectina regula negativamente el crecimiento de las células progenitoras mielomonocíticas y la producción de TNF-alfa en los macrófagos.

|
pg/ml |
D.O. |
Promedio |
Corregido |
|
|
0.00 |
0.0163 |
0.0168 |
0.0166 |
|
|
62.50 |
0.1094 |
0.1034 |
0.1064 |
0.0899 |
|
125.00 |
0.1902 |
0.2094 |
0.1998 |
0.1833 |
|
250.00 |
0.3602 |
0.3745 |
0.3674 |
0.3508 |
|
500.00 |
0.7332 |
0.7577 |
0.7455 |
0.7289 |
|
1000.00 |
1.2980 |
1.3210 |
1.3095 |
1.2930 |
|
2000.00 |
2.1300 |
2.2660 |
2.1980 |
2.1815 |
|
4000.00 |
3.2680 |
3.5890 |
3.4285 |
3.4120 |
- Los emparejamientos de anticuerpos de captura y detección optimizados con las concentraciones recomendadas ahorran un largo tiempo de desarrollo
- Se proporcionan protocolos de desarrollo para guiar una mayor optimización del ensayo.
- Alternativa económica a los kits completos
- Captura de anticuerpos
- Anticuerpo de detección
- Estándar recombinante
- Estreptavidina conjugada con peroxidasa de rábano picante (estreptavidina-HRP)
- Microplacas de 96 pocillos:AREX Biosciences, catálogo n.° DSEP01. Selladores de placas: AREX Biosciences, n.º de catálogo DSSF01.
- Tampón de recubrimiento:NaCl 137 mM, KCl 2,7 mM, Na2HPO4 8,1 mM, KH2PO4 1,5 mM, pH 7,2-7,4, fi 0,2 μm
filtrado. AREX Biosciences, catálogo n.º DSCB01. - Búfer de bloqueo: AREX Biociencias, N.º de catálogo DSBB01.
- Tampón de lavado:Tween 20 al 0,05% en PBS, pH 7,2-7,4. AREX Biosciences, catálogo n.º DSWB01.
- Tampón de ensayo:0,5% BSA, 0,05% Tween20, solución PBS. AREX Biosciences, n.º de catálogo DSAB01
Solución de sustrato:Tetrametilbencidina. AREX Biosciences, catálogo n.º DSTS01. - Detener solución:0,5 mol/ml H2SO4. AREX Biosciences, catálogo n.º DSSS01.
 Nuevos productos
Nuevos productos