Anticuerpo policlonal de conejo BCR (fosfo-Y360)
WB | 1:500 - 1:1000 |
IHC | 1:100 - 1:200 |
FI/CCI | 1:100 - 1:500 |
Descripción | Anticuerpo policlonal de conejo contra BCR (Phospho-Y360) |
Especificidad | Reconoce niveles endógenos de proteína BCR solo cuando está fosforilada en Y360. |
Tipo de anticuerpo | Anticuerpo primario |
Inmunógeno | Fosfopéptido sintético conjugado con KLH correspondiente a los residuos que rodean Y360 de la proteína BCR humana. La secuencia exacta es propietaria. |
Purificación | El anticuerpo se purificó mediante cromatografía de afinidad de inmunógeno. |
Peso Molecular | Previsto: 142 kD; Observado: 142 kD |
Formulario/búfer | Líquido en 0,42% de fosfato de potasio, 0,87% de cloruro de sodio, pH 7,3, 30% de glicerol y 0,01% de azida de sodio. |
Nombres alternativos | BCR1; D22S11; Proteína de la región del grupo de punto de interrupción; Antígeno del carcinoma renal NY-REN-26 |
Símbolo genético | BCR |
Entrez Gene | 613 (humano); 110279 (ratón) |
SwissProt | P11274 (Humano); Q6PAJ1 (ratón) |
*El número de clon, la reactividad, la fuente/host y la clonalidad se pueden encontrar en la sección de características clave y nombre del producto anterior.
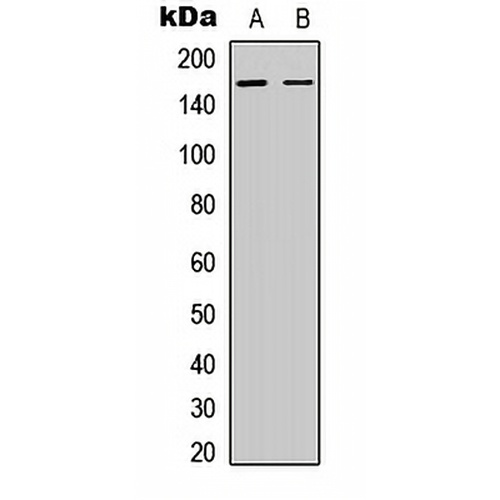
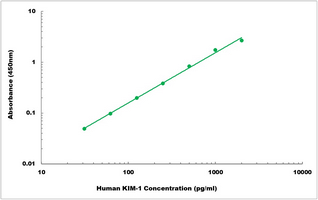
Análisis de transferencia Western de la expresión de BCR (Phospho-Y360) en lisados de células enteras de HeLa (A) y corazón de rata (B). (Tamaño de banda previsto: 142 kD; Tamaño de banda observado: 142 kD
160)
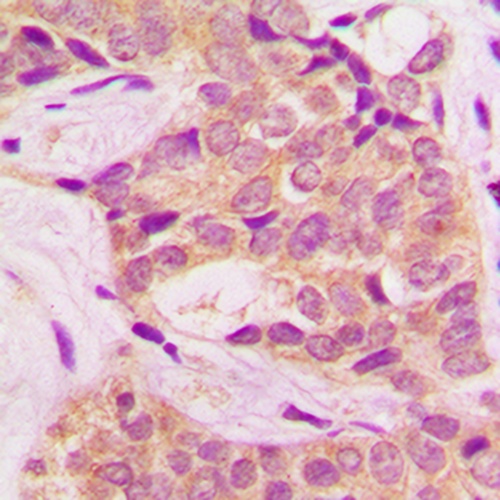
Análisis inmunohistoquímico de la tinción con BCR (Phospho-Y360) en una sección de tejido incluido en parafina fijado con formalina y cáncer de mama humano. La sección se trató previamente utilizando recuperación de antígeno mediada por calor con tampón citrato de sodio (pH 6,0). Luego, la sección se incubó con el anticuerpo a temperatura ambiente y se detectó usando un sistema de polímero compacto conjugado con HRP. Se utilizó DAB como cromógeno. Luego, la sección se contratiñó con hematoxilina y se montó con DPX.
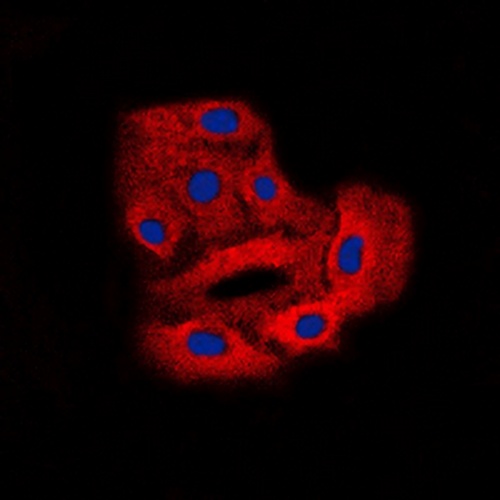
Análisis inmunofluorescente de tinción con BCR (Phospho-Y360) en células HeLa. Las células fijadas con formalina se permeabilizaron con Triton X-100 al 0,1% en TBS durante 5-10 minutos y se bloquearon con BSA-PBS al 3% durante 30 minutos a temperatura ambiente. Las células se sondaron con el anticuerpo primario en BSA al 3% - PBS y se incubaron durante la noche a 4 ° C en una cámara hidificada. Las células se lavaron con PBST y se incubaron con un anticuerpo secundario conjugado DyLight 594 (rojo) en PBS a temperatura ambiente en la oscuridad. Se utilizó DAPI para teñir los núcleos celulares (azul).
 Preguntas frecuentes
Preguntas frecuentes





 Nuevos productos
Nuevos productos




 MSDS
MSDS